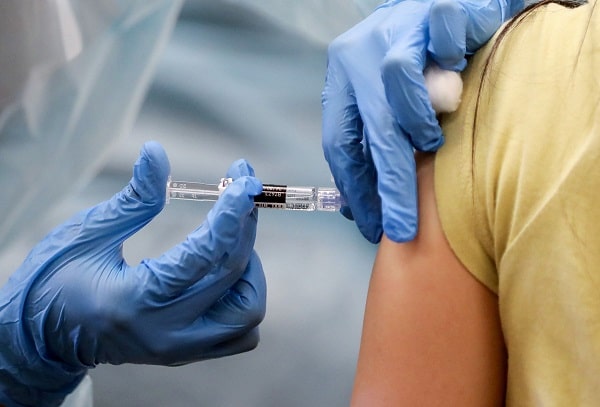
Las compañías enviarán a la FDA la solicitud de autorización para el uso de emergencia de su vacuna contra la Covid-19 por la gran eficacia que presenta.
Pfizer y BioNTech anunciaron este miércoles la finalización de la fase lll de sus ensayos clínicos de su candidata a vacuna. En las que obtuvieron valoraciones necesarias para garantizar su eficacia. Asimismo, esperan enviar una solicitud para su autorización de uso de emergencia en estos días.
El ensayo clínico llegó a 170 casos de Covid-19, donde 168 fueron administrados con un placebo y 8 recibieron la vacuna. En este se demostró un 95 % de eficacia de la vacuna a partir del día 28 después de la primera dosis.
Además, según su comunicado, planean enviar una solicitud a la Administración de Alimentos y Medicamentos de los EE. UU. (FDA). Esto con el fin de que se autorice su uso de emergencia basado en los datos obtenidos.
“Los resultados del estudio marcan un paso importante en este histórico viaje de ocho meses para presentar una vacuna capaz de ayudar a poner fin a esta devastadora pandemia. Seguimos avanzando a la velocidad de la ciencia para recopilar todos los datos recopilados hasta ahora y compartirlos con los reguladores de todo el mundo ” indicó el Dr. Albert Bourla, presidente y director ejecutivo de Pfizer.
Asimismo, Ugur Sahin, MD, CEO y cofundador de BioNTech señaló: «Estamos agradecidos de que el primer ensayo global en alcanzar la marca final de análisis de eficacia indica que se puede lograr una alta tasa de protección contra COVID-19 muy rápidamente después de la primera dosis de 30 µg, lo que subraya el poder de BNT16b2 para brindar protección temprana».
El ensayo clínico de la fase de la vacuna BNT162b2 empezó el 27 de julio y ha reunido 43,661 participantes. De estos, 41,135 han recibido una segunda dosis el 13 de noviembre de 2020. Además, se indica que «la eficacia fue constante según la edad, el género, la raza y la etnia». También, se resaltó que «la eficacia observada en adultos mayores de 65 años fue superior al 94%».
Según su comunicado, la vacuna no presenta efectos secundarios resaltantes y todos los participantes inscritos la toleraron. Algunos síntomas que se registraron son: fatiga (3,8 %) y dolor de cabeza (2 %).
Por último, esperan producir a nivel mundial hasta 50 millones de dosis en 2020 y hasta 1.300 millones de dosis para fines de 2021. Asimismo, señalaron que planean enviar los datos de eficacia y seguridad del estudio para su verificación por pares en una revista científica cuando se complete el análisis de los datos.