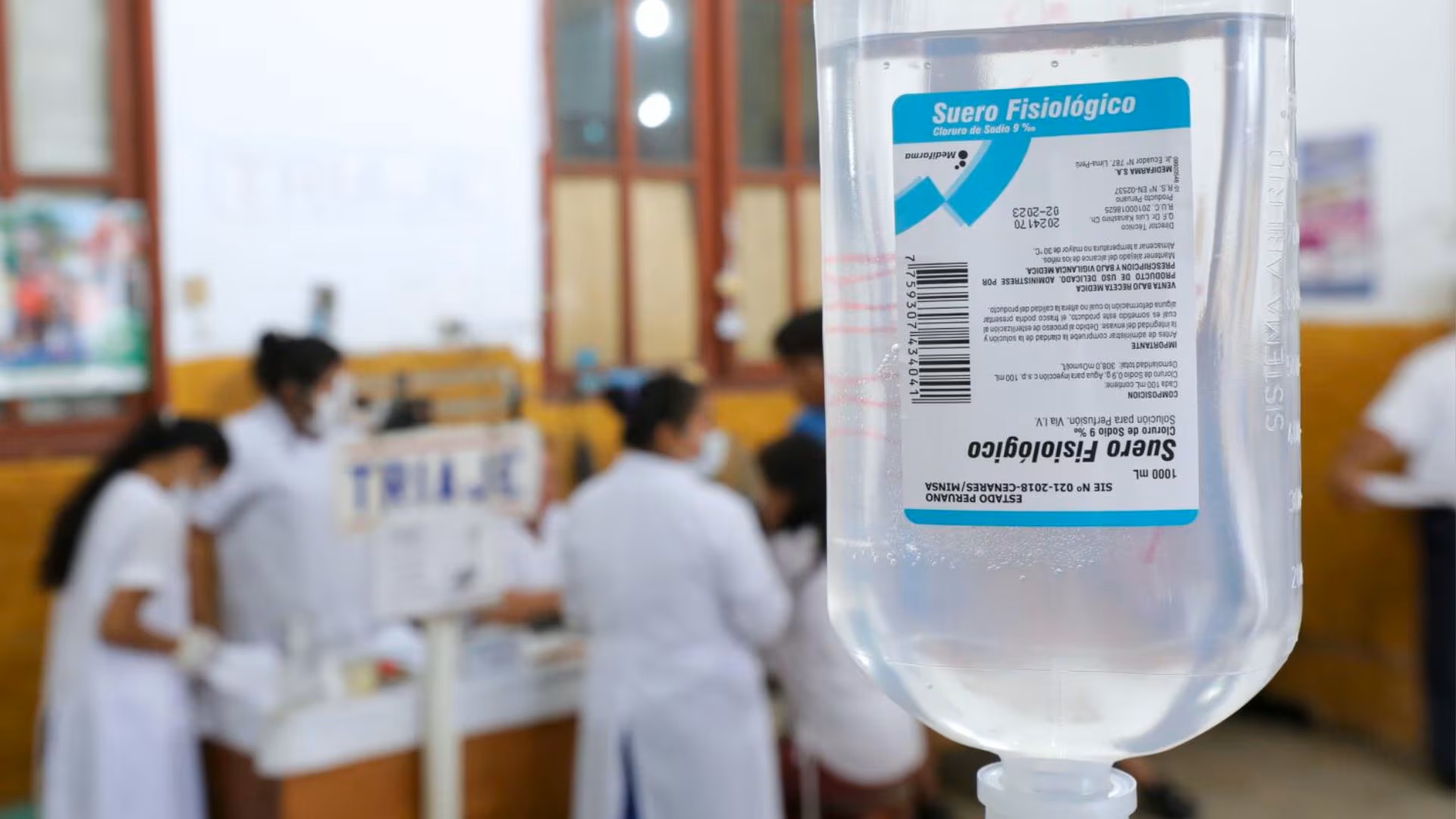
El Ministerio de Salud (Minsa), a través de la Dirección General de Medicamentos, Insumos y Drogas (Digemid), emitió una alerta sanitaria relacionada con el suero fisiológico al 0,9% producido por el laboratorio Medifarma.
Esta medida fue adoptada tras registrarse reacciones adversas graves en pacientes de diversas regiones del país. Las autoridades sanitarias alertaron que el medicamento defectuoso corresponde al lote 2123624, el cual no cumplió con el control de calidad durante su fabricación.
En los últimos días, se reportaron hasta 17 casos de pacientes afectados por el suero fisiológico: siete en estado grave y diez en estado moderado. Sin embargo, se estima que el número podría ser mayor, ya que este producto se utiliza con frecuencia en diversas prácticas hospitalarias.
DATA OFICIAL
El titular del Minsa, César Vásquez, confirmó en una conferencia de prensa relacionada con la polémica sobre el medicamento de Medifarma que, hasta la fecha, se han registrado tres muertes debido a la administración del suero fisiológico defectuoso.
“A la fecha, tenemos 17 personas afectadas por este problema. Además, dos víctimas mortales por el exceso de cloruro de sodio en la sangre y un fallecimiento que está en proceso de investigación. Es decir, son dos en La Libertad y uno en Cusco”, explicó.
No obstante, Vásquez, al ser cuestionado por la discrepancia entre la cifra de muertes que mencionó y la información proporcionada por la red Sanna, manifestó que, dado que aún están en proceso de investigación, existe la posibilidad de que haya más fallecimientos relacionados con la misma causa.
Las primeras irregularidades fueron detectadas el 22 de marzo mediante el sistema de farmacovigilancia. Al día siguiente, se reportaron dos casos graves y dos moderados en Cusco, lo que llevó a la intervención de la planta de Medifarma, donde se determinó que alrededor del 15% de los frascos analizados contenían hasta seis veces la concentración normal de la sustancia.
Ante estos hallazgos, el Minsa ordenó el cierre de las áreas de producción del insumo y, junto con Susalud, intervino los establecimientos privados que habían recibido el producto en Lima, Cusco y La Libertad. En total, se habrían distribuido cerca de 20 mil unidades del suero defectuoso.
CIERRAN PLANTA
Asimismo, precisó que la planta del laboratorio de Medifarma se encuentra cerrada hasta que culminen las investigaciones. Se indicó que se está recabando información sobre lo sucedido, pero enfatizó que la alerta solo se ha emitido para este lote.
“Se estima más de 10 mil unidades, las cuales ya fueron inmovilizadas en toda su distribución. Los reportes que hemos recibido son de La Libertad, Cusco y Lima”, agregó.
LA CAUSA
De acuerdo con el decano del Colegio Químico, Aníbal Díaz, se trataría de un fallo en el proceso de producción, lo que ha provocado que este lote no cumpla con los estándares necesarios para su uso en pacientes. Este incidente, atribuido a la omisión del control de calidad en una etapa clave, ha generado que el producto sea incompatible con las necesidades de los pacientes, lo que podría tener implicaciones significativas en su aplicación clínica.
“Su composición puede ser muy sencilla, pero debe ser elaborado en condiciones muy estrictas”, indicó el decano a Latina Noticias.
NI MINSA NI ESSALUD
Durante su declaración, César Vásquez aclaró que el lote afectado (2123624) no fue adquirido por el Minsa ni por EsSalud, por lo que se descartaron riesgos en hospitales públicos. Sin embargo, exhortó a los profesionales de salud del sector privado a revisar sus insumos y reportar cualquier anomalía.
El ministro también fue consultado sobre la continuidad de los contratos del Estado con Medifarma, empresa que ha sido proveedora de medicamentos e insumos para el sistema de salud nacional. En respuesta, señaló que, dependiendo del avance de las investigaciones, el Gobierno evaluará la posibilidad de sancionar drásticamente a la farmacéutica, lo que podría derivar en su cierre definitivo.
La Fiscalía ya ha iniciado las diligencias para esclarecer las responsabilidades en este caso. Mientras tanto, el Minsa ha reiterado su llamado a la población y al personal médico a estar alerta ante la presencia del producto en centros privados y a reportar cualquier incidente vinculado a su uso.
Multa de S/1,6 millones
La Superintendencia Nacional de Salud (Susalud) ha iniciado la investigación correspondiente sobre una presunta inadecuada atención de la clínicas y “en el cumplimiento del protocolo de atención que los pacientes recibieron frente al evento adverso de público conocimiento por la alerta Digemid”.
Indicó que las IPRESS que no acaten las disposiciones emitidas por estos organismos podrían ser sancionadas con una infracción grave con una multa de 100 a 300 UIT (S/535 mil a S/1 millón 605 mil).
Susalud dispuso de oficio “acciones inmediatas de sus órganos supervisores, en el marco de sus funciones, para la protección de los derechos en salud de la población y prevenir su vulneración, en atención a la Alerta N° 38-2025, emitida por Digemid, con fecha 24 de marzo de 2025″.